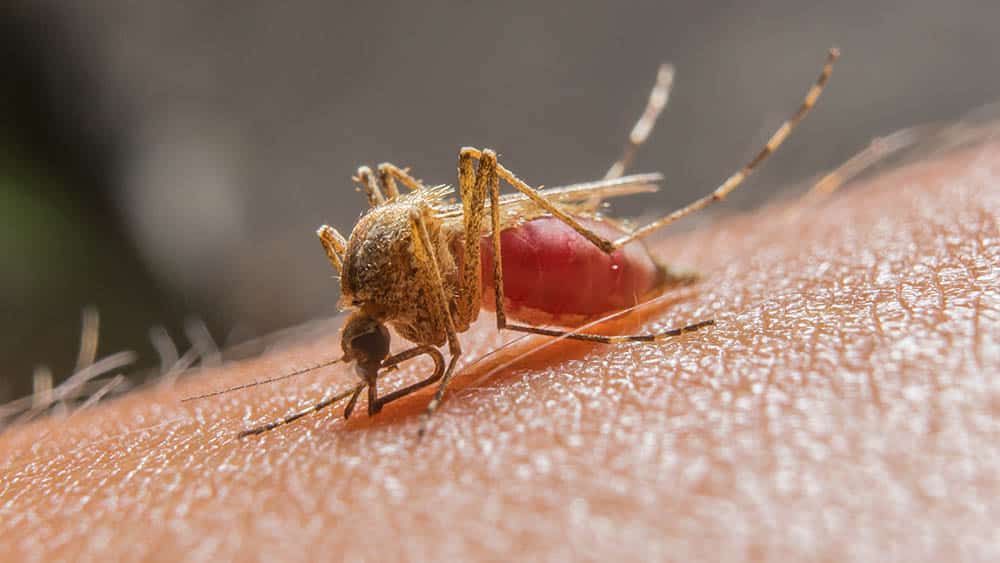
Um anticorpo monoclonal de última geração contra a malária teve um bom desempenho em segurança, eficácia, duração da meia-vida e facilidade de entrega em um estudo de fase I. Poderia este ser o santo graal para a erradicação da doença transmitida por mosquitos?
Apenas uma dose do anticorpo antimalárico L9LS conferiu proteção a 15 dos 17 receptores desafiados com infecção controlada por malária humana. Em contraste, os seis controles que não receberam o tratamento apresentaram parasitemia no teste de PCR dentro de 21 dias de exposição aos mosquitos infectados.
O L9LS mostrou uma meia-vida sérica de 56 dias, e a modelagem farmacocinética sugeriu que uma dose de 5 mg/kg em crianças pode fornecer proteção por até 6 a 12 meses, de acordo com o estudo publicado no The New England Journal of Medicine (NEJM).
“Essas descobertas podem ter importantes implicações clínicas e de saúde pública porque estabelecem o potencial de proteção avançada contra a malária em regiões com transmissão sazonal e perene”, escreveram os pesquisadores.
“A administração de uma única dose subcutânea de um anticorpo monoclonal no início da estação de transmissão pode fornecer proteção, superar problemas de adesão e potencialmente limitar o surgimento de cepas resistentes a medicamentos associadas ao uso a longo prazo da quimioprevenção da malária sazonal”, disseram eles.
Nem a administração subcutânea nem a intravenosa de L9LS foram associadas a preocupações de segurança. Os receptores relataram sintomas (por exemplo, náusea, dor de cabeça e mal-estar), que foram em grande parte leves a moderados. Um caso de linfadenopatia cervical leve ocorreu 9 dias após a administração de L9LS e se resolveu por conta própria após 29 dias, de acordo com o grupo.
O editor-chefe do NEJM, Eric Rubin, MD, PhD, especialista em doenças infecciosas, observou que o L9LS segue os passos de outro anticorpo monoclonal antimalárico que, em um estudo anterior, demonstrou não ser muito potente, exigindo grandes volumes administrados por via intravenosa em um processo caro e impraticável. Com o L9LS mais potente, “agora você pode dar esse anticorpo por via subcutânea, através de uma injeção sob a pele. É muito mais fácil, e qualquer um pode fazer isso”, Rubin afirmou em uma conferência de imprensa.
No artigo publicado, os pesquisadores contextualizam que são necessárias novas abordagens para a prevenção e eliminação da malária, uma das principais causas de doença e morte entre bebês e crianças pequenas em todo o mundo.
Eles então conduziram um ensaio clínico de fase 1 para avaliar a segurança e a farmacocinética do L9LS, um anticorpo monoclonal antimalárico de última geração, e sua eficácia protetora contra a infecção controlada por malária humana em adultos saudáveis que nunca tiveram malária ou receberam uma vacina para malária.
Os participantes receberam L9LS por via intravenosa ou subcutânea na dose de 1 mg, 5 mg ou 20 mg por quilograma de peso corporal. Dentro de 2 a 6 semanas após a administração de L9LS, tanto os participantes que receberam L9LS quanto os participantes de controle foram submetidos à infecção controlada por malária humana, na qual foram expostos a mosquitos portadores de Plasmodium falciparum (cepa 3D7).
Não foram identificados problemas de segurança. O L9LS teve uma meia-vida estimada de 56 dias, e teve linearidade de dose, com a maior média (±DP) de concentração sérica máxima (Cmax) de 914,2 ± 146,5 μg por mililitro observada em participantes que receberam 20 mg por quilograma por via intravenosa e a média de Cmax mais baixa de 41,5 ± 4,7 μg por mililitro observada naqueles que receberam 1 mg por quilograma por via intravenosa. A média de Cmax foi de 164,8 ± 31,1 nos participantes que receberam 5 mg por quilograma por via intravenosa e 68,9 ± 22,3 naqueles que receberam 5 mg por quilograma por via subcutânea.
Um total de 17 receptores de L9LS e 6 participantes de controle foram submetidos à infecção controlada por malária humana. Dos 17 participantes que receberam uma dose única de L9LS, 15 (88%) ficaram protegidos após infecção controlada por malária humana.
A parasitemia não se desenvolveu em nenhum dos participantes que receberam 5 ou 20 mg por quilograma de L9LS intravenoso. A parasitemia se desenvolveu em 1 de 5 participantes que receberam 1 mg por quilo por via intravenosa, 1 de 5 participantes que receberam 5 mg por quilo por via subcutânea e em todos os 6 participantes de controle até 21 dias após a infecção controlada por malária humana.
A proteção conferida pelo L9LS foi observada em concentrações séricas tão baixas quanto 9,2 μg por mililitro.
Neste pequeno estudo, portanto, o L9LS administrado por via intravenosa ou subcutânea protegeu os receptores contra a malária após infecção controlada, sem preocupações de segurança evidentes.
Fonte: https://doi.org/10.1056/NEJMoa2203067

