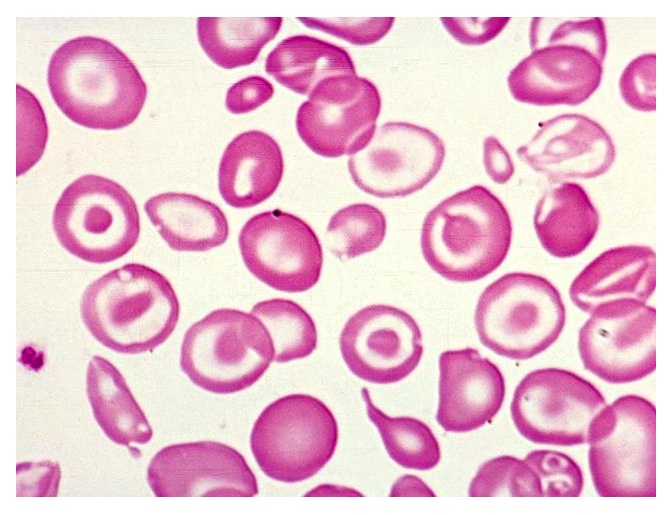
Fisiopatologia
A talassemia está entre os distúrbios mais comuns da produção de hemoglobina nas hemoglobinopatias hereditárias. Resulta de síntese do desequilíbrio da síntese da hemoglobina causada pela diminuição da produção de pelo menos uma cadeia polipeptídica da globina (beta, alfa, gama ou delta).
Talassemia alfa
A talassemia alfa resulta da redução da produção das cadeias polipeptídicas alfa decorrente da deleção de um ou mais genes alfa. As pessoas normalmente têm quatro alelos alfa (dois em cada par de cromossomos) porque o gene alfa é duplicado. A classificação da doença é feita pela quantidade e localização das deleções:
-
Talassemia: alfa+ perda de um único gene em um cromossomo (alfa/–)
-
Talassemia alfa 0: perda de ambos os genes no mesmo cromossomo (–/–)
Talassemia beta
A talassemia beta resulta da diminuição da produção das cadeias polipeptídicas beta decorrente de mutações ou deleções no gene da globina beta, levando ao comprometimento da produção de hemoglobina A. As mutações ou deleções podem resultar na perda parcial (alelo beta +) ou completa (alelo beta 0) da função da globina beta. Existem dois genes da globina beta, e os pacientes podem ter mutações heterozigóticas, homozigóticas ou heterozigóticas compostas Além disso, os pacientes podem ser heterozigotos ou homozigotos para anomalias em 2 genes diferentes da globina (p. ex., beta e delta).
Talassemia beta-delta é uma forma menos comum de talassemia beta na qual a produção tanto da cadeia delta como da cadeia beta está prejudicada. Essas mutações podem ser heterozigóticas ou homozigóticas.
Sinais e sintomas
O quadro clínico das talassemias é semelhante, mas variam em termos de gravidade de acordo com a quantidade de hemoglobina normal existente.
Talassemia alfa
Os pacientes com um único alelo alfa + são clinicamente normais (portadores silenciosos).
Os heterozigotos com defeitos em dois dos 4 genes (dois alelos alfa + ou um alelo alfa 0) tendem a apresentar anemia microcítica leve a moderada, sem nenhum sintoma. Esses pacientes têm traço talassêmico alfa.
Os defeitos em 3 dos 4 genes (co-herança de alfa + e alfa 0) comprometem muito a produção da cadeia alfa, resultando na formação de tetrâmeros com excesso de cadeias beta (hemoglobina H) ou, na infância, de cadeias gama (hemoglobina de Bart). Os pacientes com doença da Hb H normalmente mostram anemia hemolítica sintomática e esplenomegalia.
Defeitos todos os 4 genes (dois alelos alfa 0) são uma doença letal intrauterina (hidropisia fetal) porque a hemoglobina que não contém cadeias alfa não transporta o oxigênio.
Talassemia beta
Na talassemia beta, os fenótipos clínicos são classificados em 3 grupos de acordo com o grau de comprometimento da produção da globina beta:
-
Menor (ou traço)
-
Intermediária
-
Maiores
A talassemia beta menor (traço talassêmico) ocorre nos heterozigotos, que geralmente são assintomáticos com anemia microcítica leve a moderada.
A talassemia beta intermediária promove um quadro clínico variável, intermediário entre a talassemia maior e a menor.
A talassemia beta maior (ou anemia de Cooley) ocorre nos homozigotos ou heterozigotos compostos (contendo um alelo beta 0) e resulta da grave deficiência de globina beta. Esses pacientes evoluem com anemia grave e hiperatividade medular. A talassemia beta maior se manifesta em torno de 1 a 2 anos de idade com sinais e sintomas de anemia grave e sobrecarga de ferro transfusional e absortiva. Os pacientes apresentam icterícia e úlceras, podendo ocorrer colelitíase (como na doença falciforme). A esplenomegalia, quase sempre maciça, é comum. O sequestro esplênico pode se desenvolver acelerando a destruição dos eritrócitos normais transfundidos. A hiperatividade da medula óssea causa espessamento dos ossos cranianos e eminências malares. O envolvimento de ossos longos predispõe a fraturas patológicas e distúrbios no crescimento, possivelmente retardando ou impedindo a puberdade.
Com sobrecarga de ferro, os depósitos de ferro no miocárdio podem causar insuficiência cardíaca. A siderose hepática é típica, provocando distúrbio funcional e cirrose. Costuma ser necessária a quelação de ferro.
Diagnóstico
Avaliação para anemia hemolítica, se for suspeitada
-
Esfregaço periférico
-
Eletroforese de hemoglobina
-
Teste de DNA (diagnóstico pré-natal)
Traço talassêmico é comumente detectado quando o exame direto do sangue periférico de rotina e hemograma completo revelam anemia microcítica e alta contagem de eritrócitos. Se desejado, confirmar o diagnóstico de traço talassêmico beta com exames quantitativos da hemoglobina. Nenhuma intervenção é necessária.
Suspeitar de talassemias mais graves nos pacientes com história familiar, sinais ou sintomas sugestivos, ou anemia hemolítica microcítica. Em caso de suspeita de talassemia, fazer exames laboratoriais para anemia microcítica e hemolítica e exames quantitativos da hemoglobina. Os níveis séricos de bilirrubina, ferro e ferritina estão aumentados.
Nas talassemias alfas, muitas vezes o percentual de hemoglobina F e Hb A2 estão normais, e o diagnóstico dos defeitos genéticos das talassemias, em um gene ou dois genes, com frequência, pode ser feito com exames genéticos mais modernos, e normalmente como exclusão de outras causas de anemia microcítica.
Na talassemia beta maior, a anemia é grave, em geral com hemoglobina ≤ 6 g/dL. A contagem de eritrócitos é elevada em relação à Hb, pois as células são muito microcíticas. O esfregaço sanguíneo é praticamente diagnóstico, com vários eritroblastos nucleados; células-alvo; eritrócitos pequenos e pálidos; e basofilia pontilhada e difusa.
Nos métodos quantitativos de avaliação da hemoglobina, a elevação da Hb A2 é diagnóstica detalassemia beta menor. Na talassemia beta maior, a hemoglobina F costuma estar aumentada, algumas vezes chegando a até 90%, e quase sempre a hemoglobina A2 aumenta para > 3%.
A doença na Hb H pode ser diagnosticada pela demonstração da rápida migração da Hb H ou das frações de Bart na eletroforese da Hb. O distúrbio molecular específico pode ser caracterizado, mas não altera a abordagem clínica.
O estudo do DNA recombinante nos mapeamentos genéticos (particularmente PCR) se tornou padrão no diagnóstico pré-natal e no aconselhamento genético.
Se o exame da medula óssea for feito para anemia (p. ex., para excluir outras causas), mostrará hiperplasia eritroide acentuada. As radiografias obtidas por outras indicações nos pacientes com talassemia beta maior mostram alterações decorrentes da hiperatividade crônica da medula óssea. O crânio pode ter afilamento cortical, espaço diploico aumentado, aparência de raio de sol das trabéculas e aparência granular ou de cacos de vidro. Os ossos longos podem mostrar afilamento cortical, aumento no espaço da medula e áreas com osteoporose. Os corpos vertebrais podem apresentar aparência granular ou de cacos de vidro. As falanges podem aparecer retangulares ou biconvexas.
Prognóstico
A expectativa de vida é normal para as pessoas com talassemia beta menor ou talassemia alfa menor. O prognóstico da doença da hemoglobina H e da talassemia beta intermediária é variável.
A expectativa de vida é mais baixa para as pessoas com talassemia beta maior, principalmente por causa das complicações das hemotransfusões regulares.
Tratamento
-
Frequentemente, transfusão de concentrado de hemácias, com ou sem quelação do ferro
-
Esplenectomia em caso de esplenomegalia
-
Transplante de células-tronco alogênicas, se possível
Traço talassêmico alfa ou traço talassêmico beta: não tratar.
Doença da hemoglobina H: a esplenectomia pode ser útil se a anemia for grave ou em caso de esplenomegalia.
Os pacientes com talassemia beta intermediária devem receber o menor número possível de transfusões para evitar a sobrecarga de ferro. No entanto, a supressão da hematopoese anormal por transfusão periódica de eritrócitos pode ser valiosa em pacientes gravemente afetados. Na talassemia beta maior, transfundir quando houver indicação no intuito de manter a hemoglobina em torno de 9 a 10 g/dL e evitar manifestações clínicas graves. Para evitar ou retardar as complicações decorrentes da sobrecarga de ferro, o excesso (transfusional) de ferro deve ser removido (p. ex., via tratamento regular de quelação do ferro). Geralmente, iniciar a quelação quando os níveis de ferritina sérica estiverem > 1.000 ng/mL ou após cerca de um a 2 anos de transfusões programadas. A esplenectomia pode ajudar a diminuir a necessidade de transfusões em pacientes com esplenomegalia.
O transplante de células-tronco alogênicas é a única opção curativa e deve-se considerá-lo para todos os pacientes.
Pontos-chave
-
As talassemias resultam da menor produção de pelo menos uma cadeia de polipeptídeos da globina (beta, alfa, gama ou delta); os eritrócitos anômalos resultantes são microcíticos, muitas vezes com alteração morfológica e propensos à hemólise (causando anemia).
-
A esplenomegalia, frequentemente maciça, é comum e pode resultar em sequestro esplênico que acelera a destruição dos eritrócitos (incluindo aqueles transfundidos).
-
A sobrecarga de ferro é comum por causa da maior absorção (por comprometimento da eritropoiese) e das frequentes hemotransfusões.
-
Diagnosticar usando eletroforese de hemoglobina.
-
Tratar como indicado, mas monitorar a sobrecarga de ferro e usar a quelação do ferro.
-
A esplenectomia pode ajudar a diminuir a necessidade de transfusões em pacientes com esplenomegalia.
-
O transplante de células-tronco alogênicas é curativo.
Fonte:
Manual MSD


